En este weblog de Casos de ECG analizamos a 5 pacientes con síntomas potencialmente isquémicos y BRI. ¿Qué requirió activación del laboratorio de cateterismo?
Escrito por Jesse McLaren; Revisado por pares y editado por Anton Helman, julio de 2020.
Cinco pacientes presentaron síntomas potencialmente isquémicos. ¿Qué requirió activación del laboratorio de cateterismo?
Paciente 1: 90 años de historia de CAD, BRI antiguo con paro VT, cardiovertido por EMS
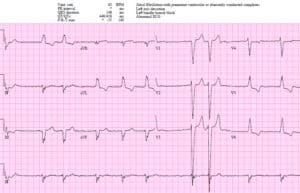

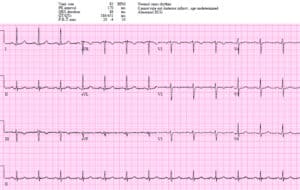
Paciente 2: 65 años con dolor bilateral en el hombro. AVSS. ECG antiguo y luego nuevo

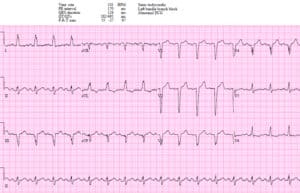

Paciente 3: 70 años con dolor en el pecho intermitente durante una semana y ahora constante. AVSS.
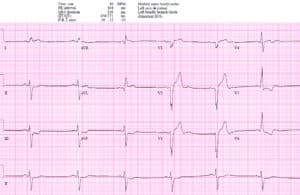

Paciente 4: 60 años/o dolor torácico de nueva aparición. AVSS
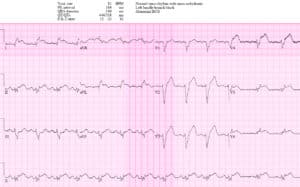

Paciente 5: Paciente de 50 años en diálisis con dolor torácico de 24 horas, AVSS, trop 1500.
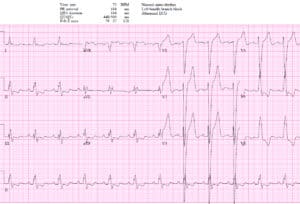

BRI + IM oclusión
La rama izquierda del haz proporciona una conducción rápida a través de los fascículos anterior y posterior. Si está bloqueado, la conducción sigue siendo rápida a través del ventrículo derecho pero se retrasa a través del ventrículo izquierdo. Por lo tanto, la despolarización es prolongada (QRS>120) y hacia la izquierda: las derivaciones anteriores tienen ondas S profundas/anchas, y las derivaciones laterales tienen ondas R borrosas o con muescas. Además, la despolarización septal inicial se invierte y se extiende de derecha a izquierda, lo que produce ondas R pequeñas o nulas en las derivaciones anteriores y desaparición de las “ondas Q septales” en las derivaciones laterales. Al igual que otras formas de despolarización anormal, el BRI produce anomalías de repolarización, y la elevación y depresión discordantes del ST han causado un dilema para el paradigma STEMI.
Como se resume en una revisión, “no sólo es difícil el diagnóstico de IAM por ECG debido al ‘enmascaramiento’ de los cambios característicos del ECG por la despolarización ventricular alterada, sino que estos pacientes pueden tener un mayor riesgo de IAM, insuficiencia cardíaca congestiva y muerte en comparación con los pacientes sin IAM. BBB.”[1] Las primeras directrices trataron a todos los pacientes con síntomas isquémicos y BRI como STEMI, según los primeros ensayos. Luego, las pautas cambiaron y consideran los “nuevos BRI” como equivalentes de STEMI, basándose en el supuesto de que se necesita un gran infarto anterior para bloquear ambos fascículos izquierdos. Pero la mayoría de los BRI no son causados por isquemia aguda sino por enfermedad cardíaca crónica, que es un issue de riesgo de SCA pero no una indicación automática para la terapia de reperfusión. Los pacientes que acuden al servicio de urgencias con síntomas isquémicos tienen tasas similares de IM, ya sea que tengan BRI nuevo, BRI antiguo o sin BRI. [2]. Tratar los “nuevos BRI” como STEMI condujo a intervenciones innecesarias, por lo que esta indicación se eliminó de las directrices de la AHA de 2013. Pero esto conduce al problema opuesto: “las directrices no reconocen que algunos pacientes con sospecha de isquemia y BRI tienen STEMI, y negar la terapia de reperfusión podría ser deadly”.[3]
Sgarbossa identificó por primera vez criterios que pueden identificar el IAM en presencia de BRI. Dado que el BRI normalmente produce STE y ETS discordantes, la isquemia aguda puede identificarse por STE concordante, ETS concordante anteriormente o STE desproporcionadamente discordante >5 mm.[4]:
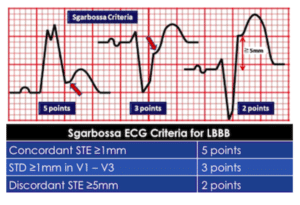

STEMI describe elevación del ST en dos derivaciones contiguas, pero Sgarbossa identificó criterios para la reperfusión aguda que incluían elevación o depresión concordantes del STE en una derivación. Pero los criterios se basaban en un IAM diagnosticado mediante enzimas, tenían un sistema de puntuación complicado y una sensibilidad y especificidad inadecuadas (en parte porque los criterios para STE desproporcionada se basaban en un valor absoluto independientemente del tamaño del QRS anterior). Smith estudió las lesiones culpables confirmadas angiográficamente e identificó criterios de ECG que pueden predecir el IM por oclusión, alejándose del paradigma STEMI y añadiendo precisión diagnóstica a los criterios de Sgarbossa. Los criterios de Sgarbossa modificados por Smith reemplazó la discordancia absoluta de >5 mm con una discordancia relativa de ST/S<-0,25 (es decir, amplitud de STE mayor que el 25 % de la amplitud de la onda S anterior), y también incluyó cualquier discordancia excesiva (ya sea STE >30 % del onda S anterior, o STD>30% onda R anterior) en cualquier derivación [5].
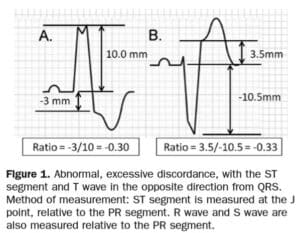

El cambio de STEMI a OMI (IM de oclusión) incluye examinar los cambios del ST (tanto elevación como depresión) en relación con el QRS anterior y en el contexto de los síntomas del paciente. Como descubrió el estudio de validación, “encontramos que los criterios de Sgarbossa modificados funcionaron igualmente bien utilizando un límite de proporcionalidad de -0,20 o -0,25. Sin embargo, como se esperaba, el límite de -0,20 produjo una sensibilidad ligeramente mayor que el límite de -0,25 (84 % frente a 80 %) y una especificidad ligeramente menor (94 % frente a 99 %). Por lo tanto, la decisión de utilizar -0,20 o -0,25 como discordancia proporcional no es absoluta sino que depende de la probabilidad previa a la prueba del médico y del contexto clínico. El ECG siempre debe utilizarse en el contexto clínico, ya que la elevación diagnóstica del ST frecuentemente está ausente en la ACO incluso en conducción regular (es decir, sin bloqueo de rama)”.[6] Cai (citado más adelante) propuso un algoritmo que tiene en cuenta los criterios de Sgarbossa/Smith, pero que comienza con el estado clínico del paciente. Al igual que con la isquemia refractaria o los pacientes hemodinámicamente inestables con conducción regular, las directrices europeas de 2017 enfatizan que “los pacientes con sospecha clínica de isquemia miocárdica en curso y BRI deben ser tratados de manera comparable a los pacientes con STEMI, independientemente de si el BRI se conoce previamente… La sospecha de isquemia miocárdica en curso es una indicación para una estrategia de ICP primaria incluso en pacientes sin elevación diagnóstica del segmento ST”.[7]
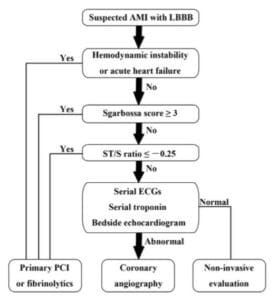

Volver a los casos
Paciente 1: activación apropiada del laboratorio de cateterismo pero sin IM de oclusión


FA con BRI, sin criterios de Sgarbossa/Smith pero paciente con alta probabilidad pretest con inestabilidad hemodinámica. Laboratorio de cateterismo activado: sin oclusión coronaria aguda.
Paciente 2: “nuevo BRI” pero activación innecesaria del laboratorio de cateterismo




Taquicardia sinusal límite con BRI nuevo en paciente estable sin criterios de Sgarbossa/Smith. Activación innecesaria del laboratorio de cateterismo, sin oclusión y trop negativo.
Paciente 3: activación retrasada del laboratorio de cateterismo


Bradicardia sinusal con BRI en paciente hemodinámicamente estable con dolor torácico continuo. STE concordante en I/aVL, ETS concordante en II/III/FAV. Omitido por dos médicos y el laboratorio de cateterismo se activó después de que trop dio positivo. Segunda oclusión diagonal. Después del stent, resolviendo cambios concordantes:

Paciente 4: adecuada activación rápida del laboratorio de cateterismo


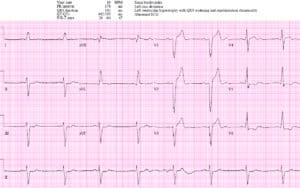
NSR con BRI en paciente hemodinámicamente estable con dolor torácico continuo. STE I/aVL/V5-6 y II concordantes y excesiva discordancia en V2 (STE/S=3/15=0,2), V3 (3/10=0,3) y V4(3/5=0,6). EMS directo al laboratorio de cateterismo: oclusión proximal de la DA que envuelve el ápice. El ECG de alta tuvo resolución de cambios de Sgarbossa/Smith:

Paciente 5: laboratorio de cateterismo activado apropiadamente pero por razones equivocadas


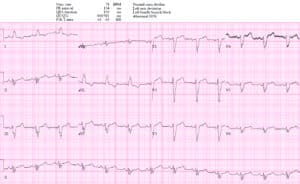
NSR con BRI interpretado por cardiología como “criterios de Sgarbossa positivos con STE >5 mm en V2-3” (lo que indicaría una possible oclusión de la DA). Pero el STE en V2-3 es proporcional a los complejos QRS masivos: STE/S en V2=6/43=0,14, V3=6/53=0,11. No existen criterios de Sgarbossa modificados para el IM por oclusión, pero el paciente tenía dolor torácico continuo con un trop positivo que requirió activación del laboratorio de cateterismo, que encontró una oclusión circunfleja (que no cumple con los criterios de STEMI en una cuarta parte de los casos, incluso en pacientes sin BRI). ).
Llévate a casa puntos por BRI + Oclusión MI
- Utilizar el Criterios de Sgarbossa modificados por Smith (STE/ETS concordantes, o STE/S excesivamente discordantes >25% o STD/R>30%) para identificar IM por oclusión en el paciente con síntomas isquémicos y BRI (ya sea nuevo o antiguo)
- Trate al paciente: aquellos con isquemia refractaria e inestabilidad hemodinámica por sospecha de infarto de miocardio por oclusión requieren activación del laboratorio de cateterismo independientemente del ECG.
Referencias para ECG Casos 11: BRI + Oclusión IM
- Neeland IJ, Kontos MC y de Lemos JA. Consideraciones en evolución en el tratamiento de pacientes con bloqueo de rama izquierda y sospecha de infarto de miocardio. J Am Coll Cardiol 2012 10 julio;60(2):96-105
- Chang AM, Shofer FS, Tabas JA, et al. Falta de asociación entre el bloqueo de rama izquierda y el infarto agudo de miocardio en pacientes sintomáticos con DE. Soy J de Emerg Med 2009;27:916-921
- Cai Q, Mehta N, Sgarbossa E et al. El enigma del bloqueo de rama izquierda en la guía sobre infarto de miocardio con elevación del segmento ST de 2013: de declarar falsamente una emergencia a negar la reperfusión en una población de alto riesgo. ¿Están listos los criterios de Sgarbossa para el prime time? Am Coronary heart J, septiembre de 2013; 166 (3): 409-13
- Sgarbossa EB, Pinkski SL, Barbagelata A, et al. Diagnóstico electrocardiográfico de infarto agudo de miocardio en evolución en presencia de bloqueo de rama izquierda. N Engl J Med 1996;334:481-487
- Smith SW, Dodd KW, Henry TD et al. Diagnóstico de infarto de miocardio con elevación del ST en presencia de bloqueo de rama izquierda con la relación entre elevación del ST y onda S en una regla de Sgarbossa modificada. Ann Emerg Med, diciembre de 2012; 60 (6): 766-776
- Meyers HP, Limkakeng AT, Jaffa EJ, et al. Validación de los criterios de Sgarbossa modificados para la oclusión coronaria aguda en el contexto de bloqueo de rama izquierda: un estudio retrospectivo de casos y controles. Am Coronary heart J, diciembre de 2015; 170 (6): 1255-64
- Ibanez B, James S, Agewall S. Directrices ESC de 2017 para el tratamiento del infarto agudo de miocardio en pacientes con elevación del segmento ST: Grupo de trabajo para el tratamiento del infarto agudo de miocardio en pacientes con elevación del segmento ST de la Sociedad Europea de Cardiología (ESC). Eur Coronary heart J, enero de 2017; 39 (2): 1119-177
¡Comparte tus casos interesantes de ECG con nosotros!
Enviar a Jesse@emergencymedicinecases.com